
帕金森病作为全球第二大神经退行性疾病,其病理机制以中脑黑质多巴胺能神经元的进行性变性死亡为核心特征。这一病理过程会直接导致纹状体多巴胺递质水平显著降低,进而使患者出现典型的运动症状,包括静止性震颤(如手部“搓丸样”抖动)、运动迟缓(如动作启动困难、步幅减小)、肌强直(如肢体被动活动时的阻力增高)等,严重影响患者的生活质量。
随着再生医学领域的蓬勃发展,干细胞疗法的兴起为神经退行性疾病的治疗带来了全新思路。这类疗法凭借干细胞具有的自我更新能力与多向分化潜能,有望通过定向诱导分化为多巴胺能神经元,实现受损神经细胞的替代与功能重建;同时,干细胞分泌的神经营养因子(如脑源性神经营养因子、胶质细胞源性神经营养因子等)还能为残存神经元提供保护微环境,延缓疾病进展。这种从神经修复角度切入的治疗策略,为突破传统药物仅能缓解症状的局限性、实现帕金森病病理层面的干预提供了重要可能性。

2025年4月,顶尖学术期刊Nature杂志同期发表了两项独立的临床研究,这两项研究聚焦于干细胞疗法在帕金森病治疗领域的应用,分别针对人诱导多能干细胞(iPSC)和人类胚胎干细胞(hESC)展开深入探索,评估其在帕金森病治疗中的安全性。
研究结果表明,iPS细胞和hES细胞来源的多巴胺能神经元前体细胞移植,有望成为一种安全且具前景的帕金森病治疗手段。


iPSC来源的多巴胺能前体细胞的I/II期试验
京都大学研究团队开展的单中心开放标签I/II期临床试验,采用HLA配型的人诱导多能干细胞(hiPSC)衍生的CORIN+多巴胺能前体细胞,对7名50-69岁的帕金森病患者进行双侧壳核移植(低剂量:2.1–2.6×10⁶细胞/侧;高剂量:5.3–5.5×10⁶细胞/侧),并开展为期24个月的随访。
试验结果显示,治疗安全性与耐受性良好,未出现严重不良事件或肿瘤形成,虽部分患者因药物调整出现轻度运动障碍加重,但免疫抑制药物(他克莫司)在15个月后停用,也未见排斥反应。疗效评估方面,6名患者中,4人的运动症状(MDS-UPDRS评分)显著改善,影像学表明壳核区¹⁸F-DOPA摄取量增加44.7%,且高剂量组的多巴胺合成增加更明显。
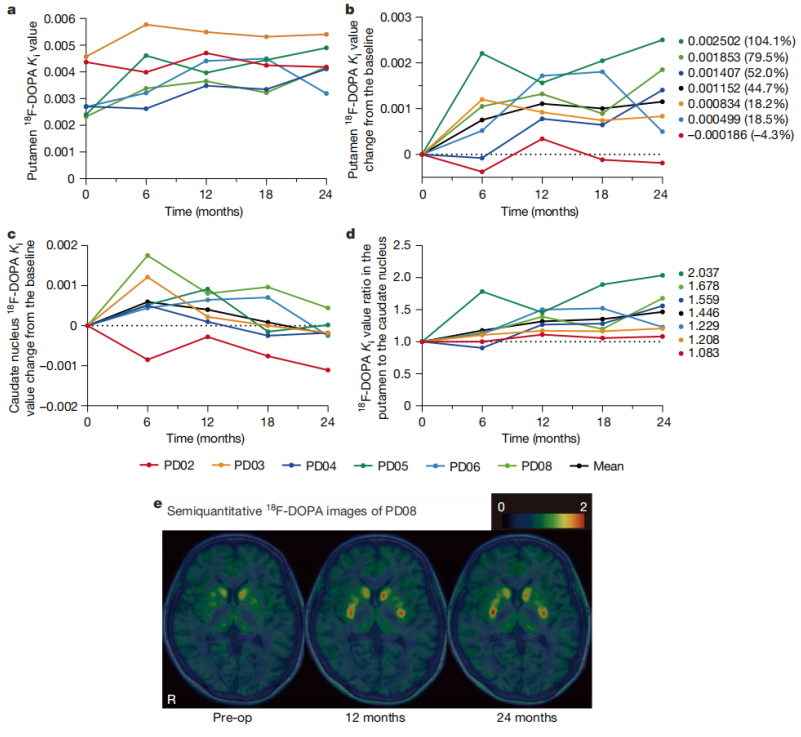
18F-DOPA PET检测DA合成
研究团队表示,后续将扩大样本量开展III期临床试验,并探索优化免疫抑制方案,以期推动该技术早日实现临床转化。
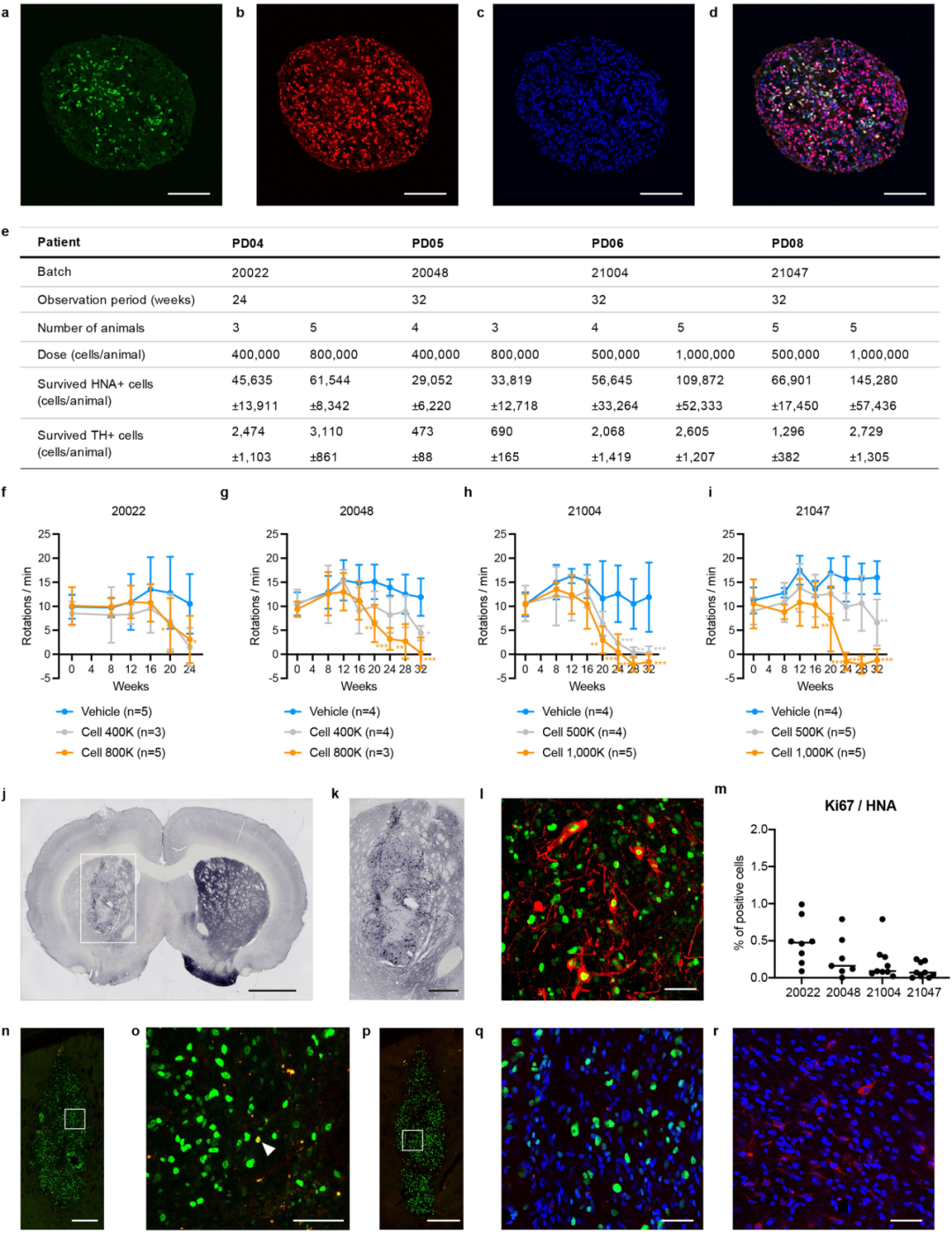
将患者使用的相同供体细胞移植
到大鼠PD模型中
1
ipsc衍生的DA祖细胞的细胞存活
hESC来源多巴胺能神经元的I期试验
纪念斯隆·凯特琳癌症中心与BlueRock Therapeutics(拜耳全资子公司)联合开展的开放标签I期临床试验,采用人类胚胎干细胞(hESC)衍生的多巴胺能前体细胞,对12名帕金森病患者进行双侧壳核区移植,其中低剂量组每侧植入0.9×10⁶个细胞,高剂量组每侧植入2.7×10⁶个细胞。
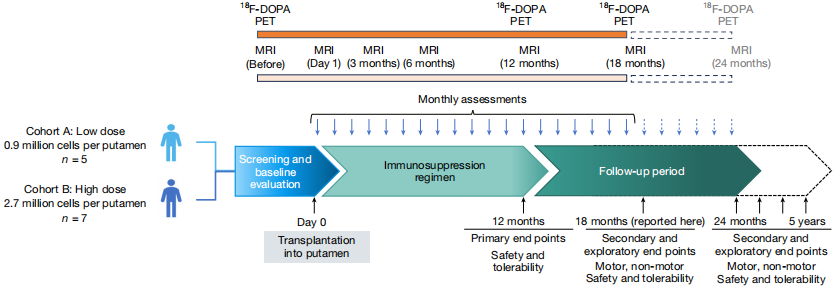
研究设计总结
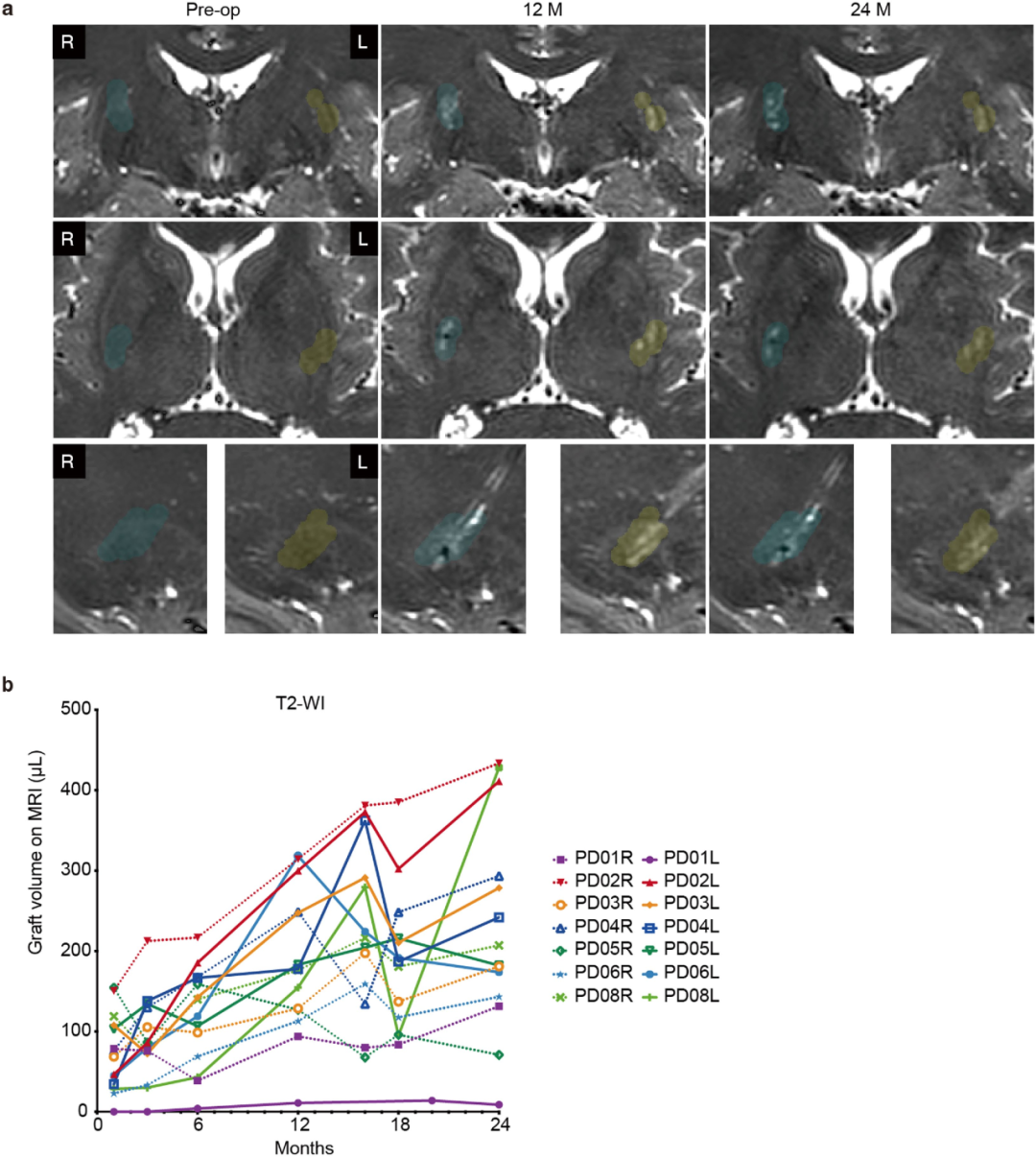
试验主要终点显示,12个月内未出现与移植物或免疫抑制相关的严重不良事件,18个月随访中未发现肿瘤或移植物诱导的运动障碍(GID)。影像学检查通过PET发现壳核区¹⁸F-DOPA摄取量增加,高剂量组更为显著;临床评分方面,高剂量组MDS-UPDRS III OFF评分较基线平均改善23分(降低35%)。患者术后1年使用他克莫司联合糖皮质激素进行免疫抑制治疗,未长期维持。
研究团队认为该细胞疗法安全性良好,为后续开展确定性临床试验提供了有力支持。
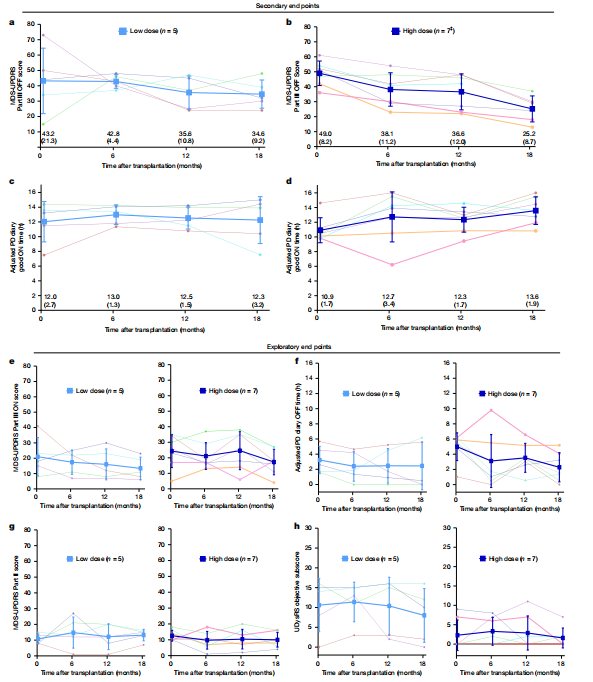
移植后18个月的临床结果
这两项临床试验均证实了干细胞衍生细胞产品异基因(非自身)移植治疗帕金森病的安全性,并显示出了初步疗效。未来还需更大规模、双盲对照试验验证长期疗效,并优化细胞剂量、移植策略及患者选择。
原文附件

1

再生医学企业在帕金森病领域也取得一定进展
2024年11月,慧心医谷对首例接受的iNSC-DAP(诱导神经干细胞来源的多巴胺能神经前体细胞)治疗的帕金森病患者进行了术后12个月的疗效评估。该患者术前罹患帕金森病8年,存在严重运动并发症,生活不能自理。治疗后,患者术后1年可独自站立和行走,姿势稳定性显著改善,生活质量明显提升。影像学分析显示,移植的多巴胺能神经细胞在患者脑内成功存活并释放神经递质,修复了受损的神经功能。此外,患者术后未出现严重不良反应,进一步证实了该治疗的安全性和显著疗效。
2024年12月20日,CDE批准了跃赛生物用于治疗原发性帕金森病的诱导多能干细胞(iPSC)来源细胞候选药物UX-DA001注射液(人中脑多巴胺能神经前体细胞注射液)的临床试验。该注射液基于跃赛生物的多能干细胞创新技术平台,包括高通量干细胞分化谱系示踪平台、高效神经分化技术平台和iPSCs重编程技术平台,能够分化出高纯度、高稳定性和高效能的人中脑多巴胺能神经前体细胞。
2025年1月14日,拜耳(Bayer)及其旗下临床阶段细胞治疗子公司BlueRock Therapeutics宣布,将启动针对帕金森病的研究性细胞疗法bemdaneprocel的III期临床试验。这项名为exPDite-2的注册临床试验预计于2025年上半年启动,将是首个用于评估帕金森病的同种异体多能干细胞衍生疗法的III期试验。bemdaneprocel是一种研究性同种异体多能干细胞衍生疗法,由多能干细胞产生的多巴胺能神经元组成,通过手术植入帕金森病患者的大脑。移植后,这些细胞可能重塑被帕金森病破坏的神经网络,从而恢复患者的运动和非运动功能。
2025年4月,士泽生物申报的1类新药通用型iPSC衍生多巴胺能神经前体细胞注射液( XS411细胞注射液)在国内获批临床,用于原发性帕金森病。此前,2025年1月,美国FDA已正式批准该药在美国开展治疗帕金森病的注册I期临床试验,FDA还授予了士泽生物帕金森病新药特殊豁免权(Exemption)。
2025年5月7日,美国生物科技公司Aspen Neuroscience公布其帕金森病自体细胞疗法药物ANPD001在ASPIRO I/IIa期临床试验中首批三名患者的6个月随访数据,结果令人振奋,该疗法在安全性、耐受性及早期疗效方面均表现优异。
帕金森病的功能性治愈一直是神经再生领域的难题,而干细胞移植正逐渐成为治疗帕金森病的突破性方法。干细胞可以分化为多巴胺能神经细胞并移植到患者大脑的特定区域,替代死亡的神经元,重建被破坏的神经网络。这种“细胞替代”疗法有望实现功能性治愈,显著改善患者的运动功能和生活质量。与此同时,AI技术的发展也为帕金森病的治疗提供了新的助力。未来,随着干细胞移植技术的优化和AI技术的进一步发展,帕金森病的治疗将更加高效和个性化,为患者带来新的希望。