
根据中国国家药监局药品审评中心(CDE)官网及公开资料不完全统计,上周(3 月 16 日 - 3 月 22 日),超 30 款 1 类创新药拟纳入优先审评/IND 获批临床默示许可/IND 申请获受理,涵盖 CAR-T、干细胞、小核酸(ASO、saRNA、siRNA)、AAV 基因疗法、溶瘤疗法、XDC、双/多抗等赛道,适应症范围不断拓宽。
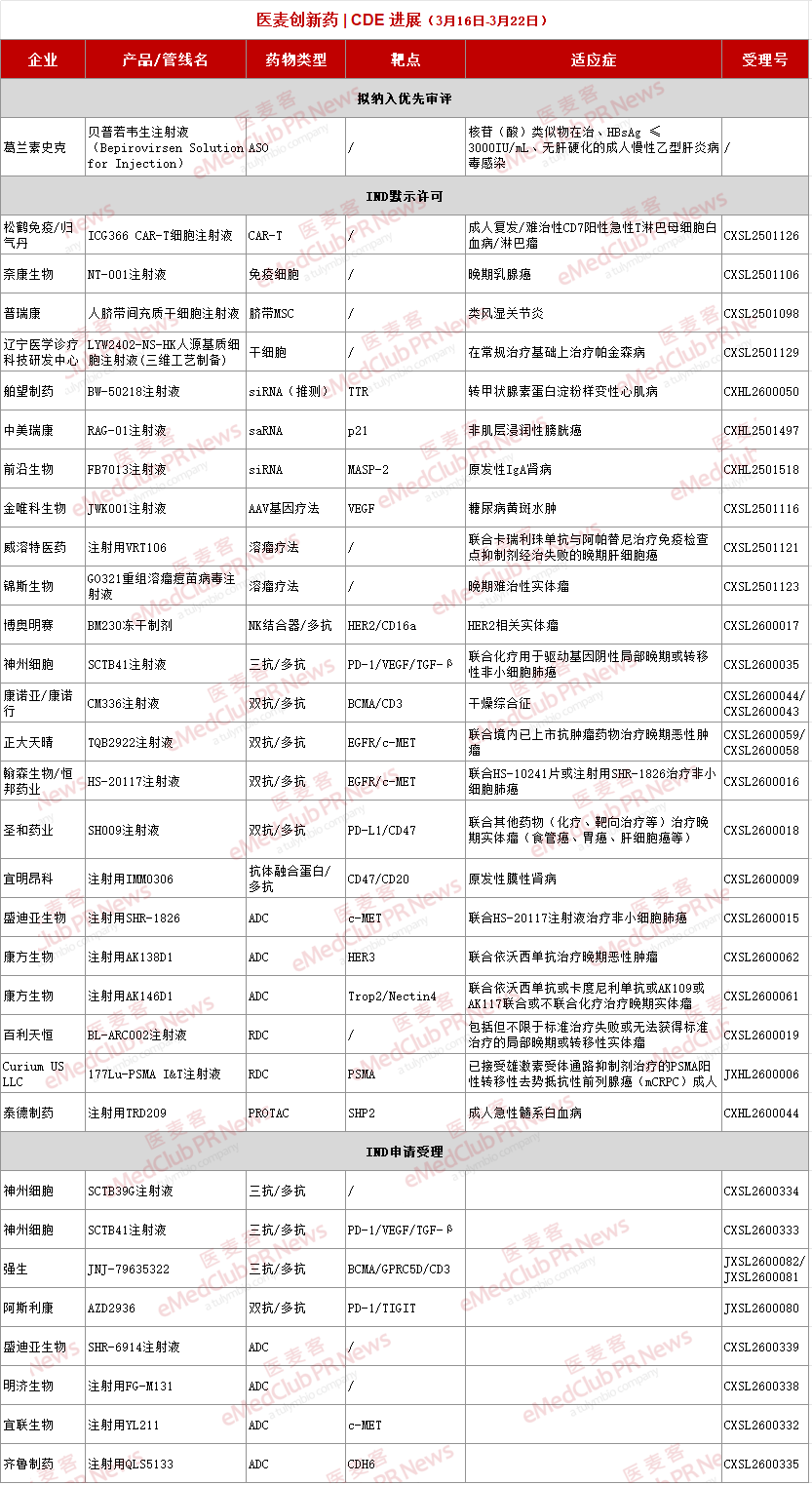 ▲ 上周获进展的 1 类创新药
▲ 上周获进展的 1 类创新药
以下是公开信息较多的代表性疗法:
奈康生物:记忆性免疫细胞
奈康生物申报的 NT-001 注射液获批临床,拟开发治疗晚期乳腺癌。该注射液是免疫细胞疗法,通过体外诱导与扩增技术,富集高比例的记忆性免疫细胞(TM 细胞),杀伤乳腺肿瘤细胞,为晚期乳腺癌患者治疗提供了一个新的选择。
辽宁医学诊疗科技研发中心:干细胞
辽宁医学诊疗科技研发中心申报的 LYW2402-NS-HK 人源基质细胞注射液(三维工艺制备)获批临床,拟定适应症为在常规治疗基础上治疗帕金森病。据公司官方披露,该注射液是首款静脉途径治疗 PD 的干细胞药物、首款以「人源基质细胞注射液」这一符合国际最新通行标准命名的细胞药物以及首款以三维全自动工艺制备的 PD 细胞药物。本次 IND 获批,有望为中晚期、药物疗效不佳的患者提供全新治疗选择。
医麦客携手艾本德中国于 2026 年 3 月 26 日(周四)19:00--20:30 带来主题为「从工艺到设备:生物药提质增效、合规可控实战分享」的直播课,邀请了艾本德中国高级产品营销经理李杰以及普健生物(武汉)科技有限公司副总经理代腾飞,将聚焦工艺路线、产质平衡、规模化放大等核心痛点,为大家带来干货分享,期待大家扫码报名参加!
中美瑞康:p21 saRNA
中美瑞康申报的 RAG-01 注射液获批开展 Ⅱ 期临床试验,拟用于治疗非肌层浸润性膀胱癌(NMIBC)。该研究的开展建立在澳大利亚 Ⅰ 期临床试验所取得的积极初步数据基础之上;现有数据显示,RAG-01 已表现出良好的安全性、明确的靶点作用证据以及抗肿瘤活性。
RAG-01 是一款特异性靶向激活肿瘤抑制基因 p21 的双链小激活 RNA(saRNA),通过 RNAa 机制激活 p21 基因的表达,以抑制肿瘤细胞增殖、诱导细胞凋亡和衰老。p21 基因在细胞周期进程中起关键调控作用,然而传统疗法却难以对其实现有效靶向。RAG-01 采用中美瑞康专有的 LiCO™ 递送技术,通过膀胱灌注给药。此前,其已于 2024 年获得美国 FDA IND 批准,并被授予快速通道资格。
前沿生物:MASP-2 siRNA
前沿生物申报的 FB7013 注射液获批临床,拟用于原发性 IgA 肾病的治疗。该注射液是靶向补体系统凝集素途径关键蛋白 MASP-2 的 GalNAc 偶联的 siRNA,通过特异性抑制 MASP-2 活性阻断凝集素途径异常激活,减少补体介导的肾脏组织损伤;基于作用机制,未来可拓展至膜性肾病、糖尿病肾病等多个补体异常激活相关疾病领域。
金唯科:AAV 基因疗法
金唯科申报的 JWK001 注射液获批临床,适应症从新生血管性年龄相关性黄斑变性(nAMD)拓展至另一高发眼科重疾领域。
据公司官网,JWK001 注射液是全球首个采用「两质粒包装系统」的 AAV 基因治疗新药,通过将携带全新自主设计的抗 VEGF 蛋白表达框的 AAV 载体,在视网膜细胞中持续高效表达抗 VEGF 蛋白,从根源上抑制眼部异常血管增生和水肿形成,有望实现一次给药、长期获益的治疗效果。
依托金唯科自主创新的核心技术平台,JWK001 在提升 AAV 载体包装效率的同时显著降低了生产成本,为其临床转化及未来商业化推广奠定了坚实基础。
威溶特:溶瘤疗法
威溶特申报的注射用 VRT106 获批开展 Ⅱ/Ⅲ 期临床试验,拟定适应症为联合卡瑞利珠单抗与阿帕替尼治疗免疫检查点抑制剂经治失败的晚期肝细胞癌。
据威溶特官网,VRT106 是全球首个基于甲病毒 M1 骨架开发的溶瘤病毒候选产品,具备三大优势:静脉注射全身给药,可更广泛地覆盖肿瘤病灶;威溶特围绕病毒受体 MXRA8 阳性和抗病毒蛋白 ZAP 阴性建立了相应的伴随诊断策略,可用于识别潜在高应答人群,推动溶瘤病毒治疗向精准化方向发展;采用高稳定性冻干粉针剂型设计,无需深低温冷链储运,在 2-8℃ 甚至室温条件下仍具备良好的稳定性。
本次获批三联方案的设计基于协同作用机制,其活性成分溶瘤病毒 M1 通过裂解肿瘤并招募 CD8+ T 细胞至肿瘤微环境,PD-1 抗体通过解除 T 细胞耗竭恢复效应功能、抗血管 TKI 通过减弱免疫抑制微环境促进免疫细胞浸润,三者协同将免疫「冷肿瘤」转化为「热肿瘤」。
在前期开展的晚期肝癌临床研究(NCT04665362)中,VRT106 联合卡瑞利珠单抗与阿帕替尼取得了较为积极的初步结果:在可评估患者中,客观缓解率(ORR)达到 70%,疾病控制率(DCR)达到 80%,中位 PFS 为 8.9 个月。