
帕金森病(PD)是全球第二大神经退行性疾病,随着全球人口老龄化进程加快,其发病率呈持续上升趋势,已成为亟待应对的重大公共卫生挑战。该病的核心病理是中脑黑质多巴胺能神经元的进行性丢失。现有左旋多巴、脑深部电刺激等手段仅能对症缓解,无法逆转神经元死亡。《Cell Biochemistry and Biophysics》与《Neurological Sciences》近期发表的两篇综述1,2,聚焦诱导多能干细胞(iPSC)在帕金森病治疗方面的应用,系统论述了iPSC疗法的价值,而全球首款iPSC疗法治疗帕金森病产品的获批,更让这一疗法从实验室研究正式走向临床应用现实。
图1 iPSC:帕金森病的再生治疗策略
iPSC疗法的核心优势
iPSC技术治疗帕金森病的核心价值在于通过将体细胞重编程为iPSC,再定向分化为功能性多巴胺能神经元,移植入脑部,替代丢失的神经元,恢复多巴胺递质功能。
两篇文献共同强调,这一策略彻底颠覆了帕金森病的治疗逻辑—不再是延缓症状,而是修复神经环路。相较于胚胎干细胞,iPSC完全规避了伦理争议;自体来源可降低免疫排斥风险,而异体场景下,通过构建“通用型”iPSC系,可大幅降低免疫排斥、缩短制备周期、降低单例治疗成本,为规模化临床应用奠定基础。更关键的是,iPSC来源的多巴胺能神经元在形态、电生理、递质释放等层面与天然中脑多巴胺神经元高度一致,移植后具备整合入宿主环路的能力。
两篇综述汇总了相关临床前证据,明确支持iPSC疗法的有效性与安全性。在6-羟基多巴胺诱导的大鼠PD模型中,移植iPSC来源多巴胺能神经元后,大鼠的运动功能显著改善,同时纹状体多巴胺释放也得到恢复。在非人灵长类动物模型中,移植的细胞不仅能长期存活,还能与宿主神经元建立功能性突触连接。
技术突破正在加速,推动临床转化
文献指出,当前,多项技术突破正在加速推进临床转化。
基因编辑正在重塑细胞来源—CRISPR/Cas9已可用于敲除HLA-I/II类分子、过表达CD47,构建低免疫原性“通用型”iPSC系,亦可校正SNCA、LRRK2、PINK1等患者特异性致病突变。
分化工艺持续优化—双SMAD抑制等方案已将分化效率显著提升,结合表面标志物流式分选,可获得高纯度、功能成熟的移植细胞。
多模式联合治疗正在探索中—基于iPSC的细胞疗法与药物干预、神经调控手段等联合应用,已在临床前模型中展现出提升移植细胞存活率与功能整合效果的潜力。
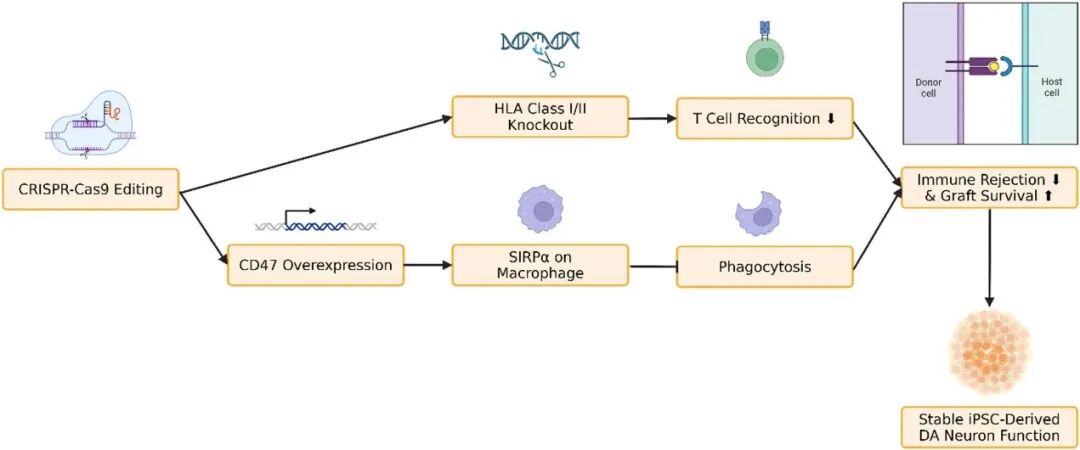
图2 CRISPR-Cas9 介导构建低免疫原性 iPSC
历史性突破:全球首批iPSC细胞疗法获批上市
基于长期的研究积累和技术工艺突破,iPSC细胞疗法迎来了重要的历史时刻。今年2月,日本厚生劳动省专家委员会正式批准了全球首批两款基于iPSC的细胞治疗产品上市。这两款疗法分别是大阪大学孵化企业Cuorips公司研发的心力衰竭治疗产品ReHeart,以及住友制药与Racthera公司合作开发的帕金森病治疗产品Amchepry。
其中,Amchepry为iPSC衍生的多巴胺能神经前体细胞(DAP)疗法,通过将iPSC定向分化为多巴胺能神经前体细胞,精准移植至患者脑内特定区域,以此重建大脑自主合成、分泌多巴胺的生理功能。
2025年5月,高桥淳教授团队在国际顶刊《Nature》上发表了这项里程碑式的研究成果,系统报告了异体iPSC来源多巴胺能前体细胞治疗帕金森病的I/II期临床试验数据。这项临床试验于2018年启动,历经7年研究,共纳入7名50-69岁的帕金森病患者。术后24个月的随访结果显示,移植细胞在大脑内存活并持续产生多巴胺,6名完成疗效评估的患者运动功能显著改善,未发生严重不良事件。
在全球首批iPSC疗法获批上市的同时,中国本土iPSC细胞疗法也在加速推进。中盛溯源开发的通用型iPSC衍生DAP疗法NCR201已进入临床II期。I期临床数据显示,NCR201在中晚期帕金森病患者中展现出良好的安全性、耐受性以及初步疗效趋势。移植后,多名患者“关期”改善、多巴胺功能PET-CT信号显著新增,以及口服多巴胺剂量下降。
总结
从《Cell Biochemistry and Biophysics》与《Neurological Sciences》两篇综述的系统佐证,到全球首款基于iPSC技术的帕金森病治疗产品Amchepry在日本成功获批上市,iPSC细胞疗法正以前所未有的速度重塑帕金森病的治疗格局。未来,iPSC疗法有望为更多存在重大未满足临床需求的疾病,为更广泛的患者带来全新的治疗希望。